El abordaje de los tumores óseos pediátricos ha experimentado una transformación profunda, consolidándose como el tercer grupo de neoplasias malignas más frecuente en la infancia y adolescencia, representando el 5% de todos los cánceres infantiles.
La supervivencia global es del 60-70% en enfermedad localizada, pero cae drásticamente al 20-30% cuando hay metástasis al diagnóstico, lo que subraya la importancia de una detección temprana.
El síntoma cardinal y principal bandera roja es el dolor óseo nocturno persistente que despierta al paciente y no cede con el reposo ni con antiinflamatorios no esteroideos (AINEs). Otros signos de alarma incluyen la presencia de una masa firme, fija y no móvil, frecuentemente en el fémur distal o la tibia proximal, así como la aparición de fracturas patológicas ante traumatismos mínimos.
Es vital diferenciar estas masas de procesos infecciosos, ya que los tumores malignos suelen carecer de signos de inflamación aguda como calor o eritema.
En la clasificación de estas patologías, es esencial distinguir entre lesiones benignas y malignas. El osteocondroma destaca como el tumor benigno más frecuente, mientras que el osteoma osteoide y el osteoblastoma presentan una tasa de recurrencia del 10-44%, siendo la radiofrecuencia guiada por TC el tratamiento de elección actual.
Entre las neoplasias malignas, el osteosarcoma es el más común, originándose en las metáfisis de huesos largos y vinculado a mutaciones en TP53 y RB1, lo que lo relaciona con síndromes como el de Li-Fraumeni. Por su parte, el sarcoma de Ewing es una entidad altamente agresiva caracterizada por células pequeñas, redondas y azules y la translocación cromosómica t(11;22) que genera la fusión EWSR1-FLI1.
Mientras el osteosarcoma suele mostrar una imagen radiográfica en sol naciente o triángulo de Codman, el sarcoma de Ewing presenta clásicamente una reacción perióstica en capas de cebolla.
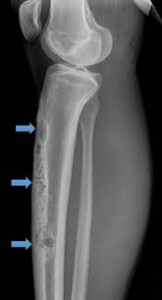
El protocolo de diagnóstico y estadificación debe ser riguroso y secuencial. La radiografía simple es la primera línea de evaluación para detectar destrucción cortical, seguida de la resonancia magnética (RM), que es el estándar de oro para delimitar la extensión local y detectar lesiones salteadas.
Debido a que los pulmones son el sitio principal de diseminación hematógena, la TC de tórax es obligatoria. Un paso crítico es la biopsia percutánea, la cual debe ser planificada exclusivamente por el cirujano oncólogo que realizará la resección definitiva, asegurando que el trayecto de la biopsia sea resecado en bloque para evitar la diseminación local del tumor.
El tratamiento actual es multidisciplinario y combina quimioterapia, cirugía y, en ocasiones, radioterapia. Para el osteosarcoma, el esquema estándar es el MAP (metotrexato, doxorrubicina y cisplatino), mientras que el sarcoma de Ewing utiliza el régimen VDC/IE. Un avance terapéutico relevante es la incorporación del mifamurtide (MTP-PE) en Europa, que ha elevado la supervivencia global.
La cirugía conservadora es ahora factible en más del 80% de los pacientes gracias a las prótesis expandibles que compensan el crecimiento óseo. Además, el sarcoma de Ewing destaca por su alta radiosensibilidad, permitiendo el uso de terapia de protones para minimizar el daño en tejidos sanos en crecimiento, a diferencia del osteosarcoma, que es fundamentalmente radiorresistente.
La oncología ha introducido avances prometedores como los inhibidores de tirosina quinasa (regorafenib, cabozantinib y pazopanib) para casos recurrentes. La terapia con células CAR-T dirigida contra HER2 ha mostrado remisiones prolongadas incluso en enfermedad metastásica pulmonar. Paralelamente, la bioingeniería tisular mediante el uso de andamiajes biológicos (scaffolds) y células madre está transformando la reconstrucción ósea postquirúrgica.
El pronóstico final del paciente depende de factores clave como la ausencia de metástasis inicial, la localización de la lesión en extremidades frente a la ubicación axial, y una buena respuesta histológica a la neoadyuvancia, definida por una necrosis tumoral mayor al 90%.
