No todo lo que silba es asma. Esta frase cobra un sentido crítico cuando nos enfrentamos a la Bronquiolitis Obliterante Postinfecciosa (BOP), una enfermedad crónica poco frecuente pero de gran impacto, que surge cuando una infección respiratoria común desencadena una cicatrización irreversible de las vías aéreas más pequeñas.
La historia de esta patología cambió radicalmente en los años 80, cuando médicos en Argentina y Chile, comenzaron a notar un aumento inusual de niños con daño pulmonar crónico tras sobrevivir a infecciones severas por virus. Lo que descubrieron fue que el daño no era solo producto del virus en sí, sino de una respuesta inmunológica desproporcionada. Hoy sabemos que existe una susceptibilidad genética específica en poblaciones como la latinoamericana, nativa americana y coreana, donde el sistema de reparación epitelial parece más propenso a generar fibrosis en lugar de una curación normal.
El Adenovirus, específicamente los serotipos 3, 7 y 21, conocido por causar neumonías necrotizantes. Aunque otros agentes como el Virus Sincitial Respiratorio o la Influenza pueden estar implicados. Otros gérmenes son:
Parainfluenza. Sarampión, Metaneumovirus humano, Virus del Herpes Simple, Citomegalovirus y Varicela-Zóster. Mycoplasma pneumoniae, Bordetella pertussis, Chlamydia pneumoniae y Legionella pneumophila.
El proceso comienza con una lesión epitelial masiva que, al intentar sanar, produce una fibrosis concéntrica que ocluye la luz de los bronquiolos, dejando el músculo liso intacto pero la vía aérea bloqueada para siempre.
Los síntomas suelen emerger tras una fase aguda de neumonía grave y deben persistir durante al menos 6 a 8 semanas. A diferencia del asma, donde los síntomas van y vienen, en la BOP la obstrucción es fija. Los niños presentan una taquipnea persistente, tos crónica no productiva y una fase de expiración prolongada que no responde a los tratamientos convencionales. Un dato estadístico revelador para el diagnóstico diferencial es la presencia de bronquiectasias, que se encuentran en el 88% de los casos de BOP, frente a solo un 29% en pacientes con asma grave.
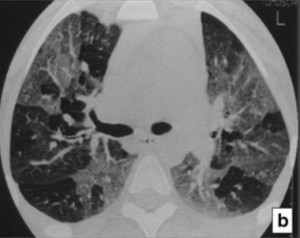
La herramienta estándar es la tomografía de alta resolución, donde aparece el signo distintivo llamado patrón de atenuación en mosaico. Al realizar una tomografía en fase espiratoria, se confirma el atrapamiento aéreo, ya que las zonas dañadas permanecen anormalmente oscuras al no poder expulsar el aire. Por su parte, la espirometría suele mostrar una mejora menor al 12% tras el uso de albuterol, confirmando que el daño es estructural y no funcional.
El manejo clínico actual se centra en controlar la inflamación residual y prevenir nuevas crisis. El tratamiento de elección suele incluir pulsos de Metilprednisolona intravenosa durante tres días al mes, un esquema que busca atacar la inflamación minimizando efectos secundarios graves como la supresión del crecimiento. Además, se utiliza la Azitromicina tres veces por semana, no por su capacidad antibiótica, sino por sus potentes efectos inmunomoduladores que ayudan a reducir la acumulación de células inflamatorias en el pulmón.
En cuanto al manejo farmacológico complementario, se suelen emplear corticosteroides inhalados a dosis altas para intentar mitigar la inflamación local y antagonistas de los receptores de leucotrienos, como el montelukast, para modular la respuesta inmune. Aunque la respuesta es limitada, se utilizan broncodilatadores de larga acción y fisioterapia respiratoria constante para mejorar el aclaramiento de secreciones y la mecánica pulmonar.
En situaciones de mayor gravedad, se ha recurrido al uso de inmunoglobulina intravenosa por su capacidad inmunomoduladora y a la suplementación de oxígeno crónica, que puede ser necesaria de forma continua o nocturna. Para los casos terminales donde el daño es incompatible con la vida, el trasplante pulmonar representa la última opción terapéutica, aunque conlleva riesgos significativos de rechazo crónico en estos pacientes.
La patología asociada más común es el desarrollo de bronquiectasias, que aparecen como consecuencia de la destrucción estructural de las vías aéreas, junto con atelectasias crónicas y neumonías bacterianas recurrentes. En algunos pacientes, la obliteración grave puede derivar en el Síndrome de Swyer-James-MacLeod, que se manifiesta como una hiperclaridad pulmonar y una disminución del flujo sanguíneo en el pulmón afectado.
Otras condiciones vinculadas incluyen el reflujo gastroesofágico, el cual debe tratarse agresivamente para evitar que las microaspiraciones agraven la lesión pulmonar. Con el tiempo, la hipoxia crónica puede generar hipertensión pulmonar y cor pulmonale, además de provocar un marcado retraso en el crecimiento y malnutrición debido al elevado gasto energético que el niño requiere para respirar.
En cuanto al futuro de estos pacientes, la evolución suele seguir la regla del 20/60/20. Un 20% de los niños logra una recuperación casi completa, mientras que el 60% mantiene una discapacidad moderada que requiere cuidados constantes pero se mantiene estable. Lamentablemente, el 20% restante enfrenta una progresión grave hacia la insuficiencia respiratoria. Debido a este riesgo, el seguimiento por neumología pediátrica debe ser obligatorio, asegurando un control estricto de la oxigenación y el cumplimiento riguroso de los esquemas de vacunación para evitar daños adicionales en un pulmón que ya ha perdido gran parte de su reserva.
