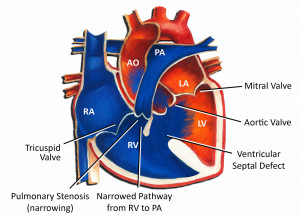
La Tetralogía de Fallot se posiciona como una de las cardiopatías congénitas cianóticas más comunes en la práctica clínica, exigiendo un conocimiento profundo para su diagnóstico y manejo oportuno. Esta condición se define por cuatro componentes anatómicos clásicos que son la comunicación interventricular (CIV), la estenosis pulmonar, la hipertrofia del ventrículo derecho y el cabalgamiento de la aorta. Es fundamental comprender que todos estos defectos derivan de una única anomalía embriológica conocida como la desviación anterior y cefálica del septo infundibular, lo cual altera la estructura normal del corazón desde su formación.
En el ámbito clínico, la presentación del paciente puede variar drásticamente según el grado de obstrucción del flujo pulmonar. Los lactantes pueden presentar episodios de cianosis que empeoran con el llanto, conocidos popularmente como crisis hipoxémicas o “TET spells”. Un signo físico muy específico en niños mayores es la adopción de la posición de cuclillas (squatting), una maniobra instintiva que aumenta la resistencia vascular sistémica para reducir el cortocircuito de derecha a izquierda y mejorar así la oxigenación. Además, a la exploración física suele destacar un soplo sistólico rudo en el borde esternal izquierdo y, en casos crónicos, la presencia de acropaquias o dedos en palillo de tambor.
Para el diagnóstico, las herramientas de imagen juegan un papel crucial. En una radiografía de tórax, el hallazgo más característico es la silueta cardiaca en forma de bota (coeur en sabot), resultado de la hipertrofia ventricular derecha que eleva el ápex y una concavidad en el segmento de la arteria pulmonar. Aunque el electrocardiograma puede mostrar una desviación del eje a la derecha, el ecocardiograma sigue siendo el estándar de oro para confirmar los cuatro componentes de la patología y planificar la intervención quirúrgica. En casos de anatomía compleja, la resonancia magnética cardiaca se vuelve indispensable para evaluar las arterias pulmonares y las colaterales aortopulmonares.
El manejo de las crisis hipoxémicas es una verdadera emergencia médica que requiere una respuesta protocolizada. El primer paso consiste en colocar al lactante en posición genupectoral (rodillas al pecho) y administrar oxígeno suplementario. Si la crisis persiste, se debe recurrir a la hidratación intravenosa, el uso de morfina para reducir el espasmo infundibular y betabloqueantes como el propranolol. En situaciones extremas donde estas medidas fallan, puede ser necesaria la administración de vasopresores como la fenilefrina o incluso una intervención quirúrgica de emergencia para crear una derivación sistémico-pulmonar.
Respecto al tratamiento definitivo, la tendencia actual es realizar la reparación quirúrgica completa entre los tres y seis meses de edad. Este procedimiento busca cerrar la comunicación interventricular y liberar la obstrucción del tracto de salida del ventrículo derecho. Es importante mencionar que algunos pacientes con síndromes asociados, como el Síndrome de deleción 22q11.2 (Síndrome de DiGeorge) o el Síndrome de Down, pueden presentar desafíos adicionales debido a anomalías inmunológicas, hipocalcemia o defectos cardiacos más complejos como el canal auriculoventricular.
A largo plazo, el éxito de la cirugía no exime al paciente de una vigilancia constante. La complicación tardía más frecuente es la insuficiencia pulmonar crónica, especialmente en aquellos que recibieron un parche transanular durante la reparación inicial. Con el tiempo, esto puede llevar a una dilatación del ventrículo derecho y la aparición de arritmias ventriculares, lo que podría requerir un reemplazo de la válvula pulmonar en la adolescencia o la edad adulta. No obstante, gracias a los avances en las técnicas quirúrgicas y el seguimiento especializado en clínicas de cardiopatías congénitas del adulto, la mayoría de los pacientes logran hoy una excelente calidad de vida y una esperanza de vida cercana a la normalidad.
