El Síndrome de Klinefelter es una de las anomalías cromosómicas más frecuentes en varones, aunque a menudo pasa desapercibida hasta etapas avanzadas de la vida. Esta condición se caracteriza por la presencia de al menos un cromosoma X extra, siendo el cariotipo 47, XXY la forma más común, presente en el 80-90% de los casos. Este material genético adicional surge generalmente por una no disyunción durante la meiosis de los padres. Aunque algunos casos se detectan prenatalmente, el momento diagnóstico más habitual es la adolescencia, cuando se hace evidente el retraso o la progresión incompleta de la pubertad.
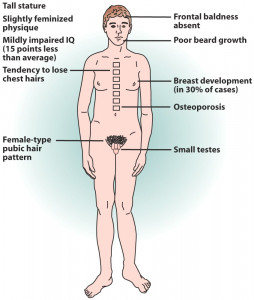
Desde el punto de vista físico, el hallazgo más consistente y fiable es la presencia de testículos pequeños y firmes, con un volumen que en la edad adulta suele ser inferior a 4 mililitros. Los pacientes suelen presentar una estatura alta con proporciones corporales específicas denominadas proporciones eunucoides, donde las piernas son desproporcionadamente largas en relación al tronco y la envergadura de los brazos supera a la altura total. Además, entre el 50% y el 70% de los afectados desarrollan ginecomastia (aumento del tejido mamario), lo que genera un malestar psicológico significativo durante la juventud.
En el ámbito del neurodesarrollo, estos niños no suelen presentar una discapacidad intelectual grave, sino que muestran dificultades de aprendizaje basadas en el lenguaje. Esto incluye retrasos en el habla, problemas con la lectura, la escritura y el procesamiento verbal. Es fundamental que el pediatra identifique estos rasgos tempranamente para iniciar terapia del habla y apoyo educativo, ya que la intervención precoz mejora drásticamente los resultados sociales y académicos a largo plazo.
El perfil hormonal del síndrome se define como un hipogonadismo hipergonadotrópico, lo que indica una insuficiencia testicular primaria. En los análisis de laboratorio, esto se traduce en niveles bajos de testosterona acompañados de una elevación compensatoria de las gonadotropinas, especialmente de la hormona folículo estimulante (FSH) y la hormona luteinizante (LH). Para confirmar el diagnóstico de manera definitiva, es indispensable realizar un análisis de cariotipo en sangre periférica, el cual permite diferenciar la forma clásica de las variantes de mosaicismo, que suelen tener un fenotipo más leve y mejor pronóstico de fertilidad.
El tratamiento de elección es la terapia de reemplazo con testosterona, la cual debe iniciarse idealmente cuando el paciente alcanza el estadio 2 de Tanner (alrededor de los 14 años) para simular una pubertad normal. El uso de geles transdérmicos diarios suele preferirse sobre las inyecciones debido a que mantienen niveles séricos más estables y evitan fluctuaciones de humor o energía. Durante el tratamiento, es vital monitorizar el hematocrito, ya que si este supera el 54% existe un riesgo elevado de trombosis, lo que obligaría a ajustar la dosis.
A largo plazo, los pacientes enfrentan riesgos metabólicos y sistémicos importantes. Aproximadamente la mitad de los adultos desarrollan síndrome metabólico, con obesidad central, hipertensión y resistencia a la insulina. Asimismo, la deficiencia crónica de andrógenos conlleva una menor densidad ósea, afectando a un tercio de los pacientes con osteoporosis. Un dato crítico para el seguimiento es que estos varones tienen un riesgo de cáncer de mama entre 20 y 50 veces mayor que la población general, por lo que cualquier masa mamaria palpable exige una evaluación inmediata.
Finalmente, el manejo de la infertilidad ha evolucionado notablemente. Aunque la mayoría de los adultos presentan azoospermia debido a la hialinización progresiva de los túbulos seminíferos que comienza en la pubertad, procedimientos como la Micro-TESE (extracción microquirúrgica de esperma testicular) permiten recuperar espermatozoides viables en cerca del 50% de los casos. Este éxito es mayor si se realiza en la adolescencia tardía o en adultos jóvenes, ofreciendo la posibilidad de tener descendencia biológica mediante técnicas de reproducción asistida con un riesgo de anomalías cromosómicas en la prole inferior al 5%.
