El desarrollo del sistema respiratorio comienza alrededor de la cuarta semana de gestación a partir del intestino anterior, mediante una compleja interacción entre el endodermo y el mesodermo. Cuando este proceso de ramificación sufre una detención focal durante la etapa pseudoglandular, se originan las malformaciones congénitas del árbol bronquial. Estas patologías tienen una incidencia estimada de 1 entre cada 2,000 a 4,000 nacidos vivos y, aunque muchas se detectan mediante ecografía prenatal en un 70-80% de los casos, su manejo requiere un conocimiento profundo de su fisiopatología.
Dentro de las patologías principales, el Quiste broncogénico destaca como la más común, presentándose como un saco ciego de epitelio respiratorio que suele ubicarse en el mediastino o cerca de la carina.
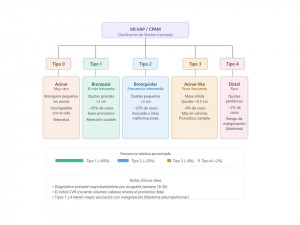
Por otro lado, la Malformación Congénita de la Vía Aérea Pulmonar (CPAM) representa un espectro que se clasifica según el tamaño de los quistes. La CPAM Tipo 1 o macrocística presenta grandes quistes mayores a dos centímetros, mientras que la CPAM Tipo 2 posee quistes de tamaño intermedio y tiene la particularidad de estar altamente asociada a otras anomalías extrapulmonares como defectos cardíacos, renales o esqueléticos. La CPAM Tipo 3 o microcística está compuesta por quistes diminutos menores a medio centímetro que, en la ecografía prenatal, reflejan las ondas de sonido creando una apariencia sólida e hiperecogénica. Finalmente, la CPAM Tipo 4 se caracteriza por quistes periféricos de pared delgada con un alto riesgo de ruptura.
Otras malformaciones incluyen la Atresia Bronquial, donde existe una obliteración focal de un segmento bronquial que genera un mucocele y atrapamiento aéreo distal, y el Enfisema Lobar Congénito, que produce una hiperinsuflación progresiva por un mecanismo de válvula. Es vital diferenciar estas entidades del Secuestro Broncopulmonar, cuya característica distintiva es que el tejido pulmonar no comunica con el árbol bronquial y recibe su irrigación de una arteria sistémica anómala procedente de la aorta.
La repercusión clínica puede ser devastadora antes del nacimiento si la masa comprime el corazón y la vena cava, reduciendo el retorno venoso y provocando hydrops fetalis, una condición con alta mortalidad que se manifiesta con ascitis y edema. Ante signos tempranos de hidropesía en lesiones microcísticas, la administración materna de betametasona puede detener el crecimiento de la masa. En casos de lesiones macrocísticas con un quiste dominante, la actitud terapéutica prenatal puede incluir la colocación de un shunt toracoamniótico para descomprimir el pulmón y permitir que el corazón bombee eficazmente.
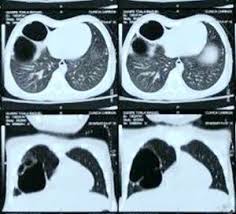
Al nacer, el neonato puede presentar un cuadro de fisiología de tensión, donde el aire entra en los quistes pero no puede salir, desplazando el mediastino y causando distrés respiratorio agudo. Sin embargo, muchos niños permanecen asintomáticos. Es un error clínico frecuente confiar en una radiografía de tórax neonatal normal, ya que los quistes pueden estar llenos de fluido y ser invisibles inicialmente. Por ello, el estándar de oro diagnóstico es la Tomografía Computarizada (TAC) con contraste entre el primer y tercer mes de vida, que permite mapear la anatomía quirúrgica y detectar vasos anómalos.
En niños mayores, estas malformaciones suelen debutar como neumonías recurrentes en la misma ubicación, tos crónica o sibilancias que no responden al tratamiento del asma, debido a que el tejido malformado carece de un aclaramiento mucociliar normal, convirtiéndose en un reservorio bacteriano. En el caso de la Tipo 4, el primer síntoma puede ser un neumotórax espontáneo por ruptura de un macroquiste periférico durante la actividad física.
La actitud terapéutica definitiva para un niño con CPAM, incluso si es asintomático, es la cirugía de resección electiva entre los 3 y 6 meses de edad. El procedimiento estándar es la lobectomía anatómica completa, ya que las técnicas que preservan parénquima como la segmentectomía tienen un mayor riesgo de resección incompleta y recurrencia. La cirugía busca dos objetivos fundamentales: prevenir infecciones graves y eliminar el riesgo de transformación maligna en blastoma pleuropulmonar o adenocarcinoma. Si se detectan elementos de blastoma en la patología, es obligatorio realizar pruebas genéticas para la mutación DICER1, que predispone a otros tumores familiares. Una complicación postoperatoria grave a vigilar es la fístula broncopleural, que se manifiesta por un burbujeo continuo en el tubo de tórax y requiere revisión urgente.
En la actualidad, la cirugía puede realizarse mediante una toracotomía tradicional o a través de cirugía torácica asistida por video (VATS), una técnica mínimamente invasiva que reduce el dolor postoperatorio y mejora el resultado estético, un factor relevante para la autoimagen del niño.
Durante el procedimiento, la precisión técnica es crítica, especialmente en el control vascular y el cierre del muñón bronquial. En casos de secuestro broncopulmonar, el cirujano debe identificar y ligar con extrema cautela la arteria sistémica anómala que proviene directamente de la aorta, ya que su sección accidental podría provocar una hemorragia masiva. Una vez completada la exéresis, el espacio vacío dejado por el lóbulo extirpado no permanece hueca; la biología pediátrica permite un crecimiento pulmonar compensatorio, donde los lóbulos restantes aumentan su número de alvéolos y su volumen para ocupar el espacio y restaurar la función respiratoria total.
No obstante, como toda intervención de alta complejidad, la cirugía no está exenta de riesgos y complicaciones postoperatorias. La más temida es la fístula broncopleural, que ocurre cuando el cierre del bronquio principal del lóbulo extirpado falla, permitiendo una comunicación directa entre la vía aérea y el espacio pleural. Esto se manifiesta clínicamente por un burbujeo continuo y masivo en el sistema de drenaje torácico y requiere, en la mayoría de los casos, una reintervención urgente para sellar la fuga. Otras complicaciones incluyen el neumotórax persistente por fugas aéreas menores desde la superficie del pulmón remanente, el quilotórax por lesión accidental del conducto torácico durante la disección, y la neumonía postoperatoria si el niño no logra realizar una expansión pulmonar adecuada debido al dolor.
La cirugía elimina el riesgo futuro de malignización o infecciones graves.
El cuerpo posee una capacidad de crecimiento pulmonar compensatorio extraordinaria, lo que garantiza que tras la cirugía podrán llevar una vida física normal, reforzando su seguridad y autoestima.