La dermatomiositis juvenil (DMJ) es una enfermedad autoinmune sistémica rara en la que el sistema inmunitario del niño ataca principalmente la piel, los músculos y los vasos sanguíneos, afectando aproximadamente a 3 niños por millón al año, generalmente con una edad de inicio entre los 5 y 10 años.
Esta patología se caracteriza por ser una condición en la que la mayoría de los pacientes no responden completamente a la terapia inicial, presentando a menudo un curso crónico refractario o policíclico.
Los principios rectores para su manejo clínico son el reconocimiento temprano, el tratamiento oportuno y la prevención de daños, basándose en que la DMJ es fundamentalmente una vasculopatía más que una miopatía primaria.
Su secuencia fisiopatológica comienza con la regulación al alza de los interferones tipo 1, los cuales activan la cascada del complemento, provocando el depósito del complejo de ataque a la membrana C5b-9 en el endotelio capilar, lo que deriva en lesión endotelial, pérdida capilar progresiva, atrofia muscular perifascicular y vasculopatía cutánea. A diferencia de la versión adulta, el riesgo de malignidad en la infancia es muy bajo.
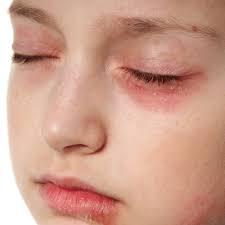
En cuanto a la presentación clínica, existen lesiones cutáneas patognomónicas esenciales para el diagnóstico. El eritema en heliotropo consiste en una coloración violácea, púrpura o lila de la piel periorbitaria y los párpados superiores, frecuentemente acompañada de edema palpebral. Las pápulas de Gottron son pápulas violáceas, escamosas y elevadas sobre las superficies extensoras de las articulaciones, especialmente en nudillos, codos, rodillas y tobillos; estas deben diferenciarse del signo de Gottron, que es un eritema macular plano no elevado.
Es vital distinguir estos hallazgos de otros cuadros: el eritema malar que afecta los pliegues nasolabiales indica lupus eritematoso sistémico, el eritema asalmonado evanescente señala artritis idiopática juvenil sistémica y el eritema marginado se asocia a la fiebre reumática aguda.
La afectación muscular en la DMJ se caracteriza por una debilidad de los grupos musculares proximales en un patrón simétrico, afectando la cintura escapular y pélvica, lo que provoca dificultad para levantar los brazos, un signo de Gower positivo y marcha de ánade.
La debilidad de los flexores del cuello se manifiesta como caída de la cabeza o incapacidad para levantarla de la almohada. Un signo de peligro crítico es la debilidad faríngea que causa disfagia, lo que requiere intervención urgente por riesgo de aspiración.
Para la evaluación formal de la fuerza se utiliza la Escala de evaluación de miositis infantil (CMAS). Asimismo, la capilaroscopia del lecho ungueal permite observar de forma no invasiva la microangiopatía mediante asas capilares dilatadas, hemorragias y áreas avasculares, lo cual correlaciona directamente con la actividad de la enfermedad.
Los anticuerpos específicos de miositis son determinantes para el pronóstico y la personalización del tratamiento. El anticuerpo anti-MDA5 se asocia fuertemente con la enfermedad pulmonar intersticial rápidamente progresiva (con una mortalidad hasta del 50% en casos refractarios), úlceras cutáneas y enfermedad amiopática. El anti-NXP2 está vinculado a la calcinosis y enfermedad muscular grave. El anti-TIF1-gamma se relaciona con afectación cutánea severa y fotosensibilidad, requiriendo cribado de cáncer incluso en niños. El anti-Mi-2 se asocia con la erupción clásica y una respuesta favorable a los esteroides, mientras que el anti-Jo-1 es raro en pediatría.
Para el diagnóstico, la biopsia muscular con histopatología es el estándar de oro, mostrando atrofia perifascicular, inflamación perivascular (linfocitos T CD4+ y células B) y pérdida capilar. La resonancia magnética (secuencias STIR) es altamente sensible para detectar edema muscular y guiar el sitio de la biopsia. En el laboratorio se observan elevaciones de la creatina quinasa (CK), lactato deshidrogenasa (LDH), aldolasa y transaminasas, aunque la CK puede ser normal en algunos casos. Los criterios de clasificación EULAR/ACR 2017 utilizan un sistema de puntos basado en hallazgos cutáneos, debilidad proximal, enzimas musculares, disfagia y resultados de biopsia o resonancia.
El tratamiento de primera línea tiene como objetivos eliminar la inflamación, restaurar y preservar el rendimiento muscular y prevenir la discapacidad. Consiste en la combinación de corticosteroides sistémicos a dosis altas (prednisona oral o pulsos de metilprednisolona intravenosa) junto con metotrexato (preferiblemente subcutáneo), considerado el mejor tratamiento inicial para la mayoría de los niños. Los síntomas pueden comenzar a mejorar en 2 a 4 semanas. Es obligatorio el uso de protección solar, suplementos de calcio y vitamina D, además de fisioterapia y rehabilitación constante para reforzar los músculos, mejorar el rango de movimiento y evitar contracturas. Se puede utilizar hidroxicloroquina como adyuvante para la erupción cutánea.
Como tratamientos de segunda línea o ante una enfermedad refractaria, las opciones incluyen inmunoglobulina intravenosa (IGIV), que contiene anticuerpos sanos que bloquean la acción de los anticuerpos perjudiciales y es especialmente útil en casos de disfagia. También se emplean la azatioprina, ciclosporina, tacrolimus, micofenolato de mofetilo (MMF) y biológicos anti-TNF. En casos de mayor gravedad o falta de respuesta a terapias convencionales, se utiliza el rituximab (anticuerpo monoclonal anti-CD20) o la ciclofosfamida intravenosa.
En el área de terapias biológicas emergentes, el mayor avance reside en los inhibidores de JAK (tofacitinib, baricitinib, ruxolitinib, upadacitinib), que interfieren con la señalización de los interferones tipo I. El 71,4% de los pacientes tratados con tofacitinib logró suspender los glucocorticoides. Otros biológicos en uso incluyen el abatacept, tocilizumab y agentes anti-interleucina-1. El horizonte investigador se centra actualmente en terapias dirigidas a células B y a la disfunción mitocondrial. En pacientes con anti-MDA5 y enfermedad pulmonar intersticial, los inhibidores de JAK han mostrado resultados muy prometedores.
Las complicaciones de la DMJ pueden ser devastadoras. La calcinosis cutis (depósitos de hidroxiapatita de calcio en piel, músculo y fascia) afecta al 30-70% de los pacientes, especialmente a los positivos para anti-NXP2; se han intentado tratamientos con bifosfonatos o diltiazem, pero no existe una cura probada, por lo que el control agresivo temprano es la mejor prevención.
La vasculopatía gastrointestinal representa una emergencia médica por riesgo de isquemia, ulceración y perforación intestinal. Finalmente, la lipodistrofia asociada a síndrome metabólico ocurre en el 10-20% de los casos, provocando distribución anormal de la grasa, resistencia a la insulina, hipertrigliceridemia y acantosis nigricans, lo que aumenta el riesgo cardiovascular a largo plazo.
La tendencia actual se dirige firmemente hacia estrategias personalizadas según el perfil de autoanticuerpos para guiar la elección terapéutica y anticipar complicaciones.
