Síndrome de Cushing en Pediatría
El síndrome de Cushing representa un desafío diagnóstico en la práctica clínica.
Uno de los signos más tempranos y críticos es el patrón de crecimiento. En un caso típico, una niña de 10 años presenta una ganancia de peso de 15 kg en pocos meses, concentrada principalmente en la zona central. A diferencia de la obesidad simple, donde los niños suelen tener una talla alta para su edad, el síndrome de Cushing pediátrico se caracteriza por una desaceleración del crecimiento lineal. Si un paciente presenta un aumento de peso significativo mientras cae en los percentiles de estatura, este hallazgo es prácticamente patognomónico y debe encender las alarmas de hipercortisolismo.
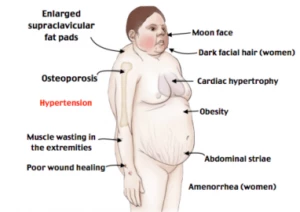
Los cambios faciales son distintivos. La cara de luna llena es el resultado de la redistribución anormal de la grasa, mientras que la plétora facial ocurre debido al adelgazamiento de la piel y al aumento de la visibilidad de los vasos sanguíneos. Es común observar también la presencia de acné y vello terminal, lo que refleja el exceso de andrógenos que suele acompañar a la elevación del cortisol. Otros signos físicos clave incluyen la giba de búfalo (almohadilla de grasa en la base posterior del cuello) y las almohadillas de grasa supraclaviculares, que contrastan con extremidades notablemente delgadas debido al catabolismo muscular.
La piel del paciente con Cushing es extremadamente frágil. Las estrías violáceas son marcas de color púrpura, típicamente mayores de 1 cm de ancho, que aparecen en el abdomen y los muslos. El cortisol en exceso inhibe la síntesis de colágeno, provocando que la dermis se desgarre ante el aumento de peso. A nivel muscular, los pacientes suelen experimentar miopatía proximal, que se manifiesta como dificultad para subir escaleras o levantarse de una silla sin usar los brazos (el llamado signo de la silla). Además, el hueso sufre gravemente: el cortisol reduce la función de los osteoblastos, lo que disminuye la formación ósea y conduce a una osteoporosis severa y fracturas ante traumas mínimos.
El impacto sistémico es profundo. Aproximadamente el 80% de los casos pediátricos presentan hipertensión arterial, causada por el efecto mineralocorticoide del cortisol, que retiene sodio y agua, y por el aumento de la sensibilidad vascular a los vasopresores. A largo plazo, esto provoca hipertrofia ventricular izquierda y riesgo de insuficiencia cardíaca. Por otro lado, entre el 20% y el 40% de los pacientes desarrollan diabetes esteroidea debido al aumento de la gluconeogénesis hepática y la resistencia periférica a la insulina. Asimismo, el estado de inmunosupresión aumenta significativamente el riesgo de infecciones fúngicas y oportunistas.
El diagnóstico comienza con la confirmación del hipercortisolismo. El cortisol salival nocturno es una prueba de cribado excelente y no invasiva, ya que detecta la pérdida del ritmo circadiano normal (el cortisol debería ser mínimo a medianoche). Una vez sospechado, se puede confirmar con el cortisol libre urinario de 24 horas, donde niveles cuatro veces superiores al límite normal son confirmatorios.
Tras confirmar el exceso de cortisol, el siguiente paso es medir la ACTH plasmática. Si la ACTH está baja, el origen es probablemente un tumor adrenal. Si la ACTH está elevada, estamos ante un cuadro dependiente de ACTH, que puede ser la enfermedad de Cushing (un adenoma hipofisario, causa del 60-70% de los casos pediátricos) o, más raramente, un tumor ectópico. En casos de enfermedad de Cushing, la prueba de supresión con dexametasona en dosis altas suele mostrar una reducción del cortisol mayor al 50%, ya que los adenomas hipofisarios conservan una respuesta parcial al feedback negativo.
Tratamiento
El tratamiento de elección para la enfermedad de Cushing es la cirugía transesfenoidal. Curiosamente, el éxito quirúrgico se predice por la aparición de hipocortisolismo postoperatorio inmediato; un nivel de cortisol muy bajo indica que el tumor ha sido removido completamente. Estos pacientes requerirán reemplazo con hidrocortisona durante meses hasta que el eje adrenal se recupere. Es vital educar a las familias sobre el dosis de estrés, triplicando la dosis de hidrocortisona en caso de fiebre o enfermedad para evitar una crisis adrenal.
En casos de tumores adrenales malignos como el carcinoma cortical adrenal, se observa una masa grande, irregular y con invasión local en las imágenes, lo que requiere una resección quirúrgica agresiva. Si la cirugía hipofisaria falla, las opciones incluyen la radioterapia hipofisaria (que tarda de 6 a 18 meses en hacer efecto) o la adrenalectomía bilateral, que cura el hipercortisolismo de forma inmediata pero crea una insuficiencia adrenal permanente y conlleva el riesgo de desarrollar el síndrome de Nelson. Para el control preoperatorio agudo, medicamentos como la metirapona son eficaces para bloquear la síntesis de cortisol y estabilizar al paciente antes de la intervención definitiva.
