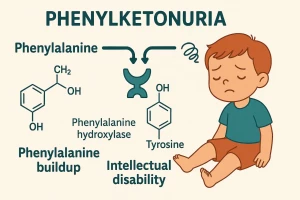
La fenilcetonuria, conocida comúnmente como PKU, representa uno de los errores innatos del metabolismo más significativos y relevantes en la pediatría actual.
Su importancia radica en que, a pesar de su potencial gravedad, es una condición tratable cuya detección temprana y manejo constante pueden cambiar por completo el destino neurológico de un paciente. Esta patología se origina por la deficiencia o mal funcionamiento de la enzima fenilalanina hidroxilasa, encargada de convertir el aminoácido fenilalanina en tirosina. Cuando este proceso falla, la fenilalanina no se metaboliza correctamente y se acumula a niveles tóxicos en la sangre, provocando daños devastadores en el tejido cerebral, retraso del desarrollo intelectual y graves alteraciones neuropsiquiátricas si no se interviene de manera inmediata.
El primer paso crítico en la vida de un recién nacido es el tamiz neonatal, una prueba de cribado que debe realizarse idealmente entre las 24 y 72 horas posteriores al nacimiento. Un error común en la práctica clínica es realizar la prueba demasiado pronto, antes de que el bebé haya ingerido suficiente proteína a través de la alimentación, lo que puede derivar en un falso negativo peligroso. Es fundamental que el personal médico comprenda que un resultado alterado en el tamiz no constituye un diagnóstico definitivo, sino una alerta que exige una confirmación mediante niveles plasmáticos de aminoácidos para determinar el fenotipo específico del paciente y la relación entre fenilalanina y tirosina.
Si el diagnóstico se retrasa, el cuadro clínico clásico comienza a manifestarse de forma evidente entre los tres y seis meses de edad. Los padres suelen notar una hipopigmentación progresiva, caracterizada por piel muy clara, ojos azules y cabello rubio, incluso en familias con rasgos físicos oscuros. Este fenómeno ocurre porque la falta de tirosina impide la producción normal de melanina. Además, es frecuente detectar un olor corporal característico a moho o ratón, provocado por la excreción de metabolitos tóxicos que el cuerpo genera al intentar procesar el exceso de fenilalanina. Desde el punto de vista neurológico, el impacto es profundo, ya que la deficiencia de neurotransmisores como la dopamina y la norepinefrina explica la aparición de síntomas como hipotonía, irritabilidad, temblores y retraso global del desarrollo.
El objetivo central del tratamiento es mantener las concentraciones sanguíneas de fenilalanina dentro del rango terapéutico, y para ello la piedra angular sigue siendo el tratamiento dietético. Seguir una dieta baja en fenilalanina de por vida implica una restricción severa de proteínas naturales, las cuales deben sustituirse por fórmulas de aminoácidos sintéticos. Una alternativa innovadora es el glicomacropéptido, una proteína de origen bovino con niveles mínimos de fenilalanina que ofrece una fuente de proteína intacta, siendo más adecuada para la etapa adulta que para la infancia.
Más allá de la dieta, la medicina moderna ha incorporado opciones farmacológicas de gran valor. La sapropterina (Kuvan®) actúa como un cofactor de la enzima PAH y es efectiva en pacientes con formas leves o moderadas que conservan cierta actividad enzimática residual. Por otro lado, para la población adulta con PKU no controlada, se dispone de la pegvaliasa (Palynziq®), una terapia enzimática sustitutiva que utiliza una enzima bacteriana para metabolizar la fenilalanina directamente en el torrente sanguíneo, reduciendo sus niveles de forma duradera.
El avance más relevante es la autorización de la sepiapterina (Sephience®). Esta molécula marca un punto de inflexión gracias a su mecanismo de acción dual: funciona como un precursor que el cuerpo transforma intracelularmente en BH4 y, al mismo tiempo, actúa como una chaperona farmacológica que corrige el plegamiento incorrecto de la enzima PAH. Datos recientes indican que casi la totalidad de los pacientes tratados con sepiapterina pueden aumentar significativamente su ingesta diaria de proteínas naturales manteniendo un control metabólico óptimo, lo que promete tratar un espectro mucho más amplio de pacientes.
Un aspecto de vital trascendencia es el manejo de la fenilcetonuria materna. Las mujeres con PKU que desean ser madres deben alcanzar un control metabólico riguroso antes de la concepción y mantenerlo durante todo el embarazo, idealmente entre 120 y 360 µmol/L. Los niveles elevados de fenilalanina en la madre atraviesan la placenta y son extremadamente tóxicos para el feto, pudiendo causar microcefalia, defectos cardíacos congénitos y discapacidad intelectual. El monitoreo durante la gestación debe ser intensivo, realizándose análisis de sangre de forma recurrente para garantizar un entorno seguro para el desarrollo fetal.
El horizonte futuro de la enfermedad es esperanzador con el desarrollo de terapias génicas y técnicas de edición genómica como CRISPR/Cas9, que buscan corregir el defecto genético de raíz. Otras líneas de investigación incluyen el uso de aminoácidos neutros de gran tamaño (LNAA) para bloquear la entrada de fenilalanina al cerebro, el desarrollo de probióticos que mejoren la actividad metabólica en el duodeno y técnicas de degradación intestinal de la fenilalanina para evitar las restricciones dietéticas.
Finalmente, el éxito a largo plazo depende de la transición exitosa a la adolescencia y la edad adulta, etapas donde la presión social suele comprometer la adherencia al tratamiento. El riesgo de deterioro cognitivo y trastornos del estado de ánimo persiste si se abandona el control, por lo que el apoyo psicológico y la educación estructurada son componentes esenciales del equipo multidisciplinario. En última instancia, la integración de la dieta clásica con las nuevas terapias como la sepiapterina permite que los pacientes con PKU vislumbren un futuro con mayor libertad alimentaria y una salud neurológica preservada.
