La ataxia-telangiectasia, también conocida clínicamente como Síndrome de Louis-Bar, se define como un trastorno neurodegenerativo multisistémico de herencia autosómica recesiva que afecta aproximadamente a uno de cada 40,000 a 100,000 nacimientos.
Esta patología es causada por mutaciones en el gen ATM (Ataxia-Telangiectasia Mutated) localizado en el cromosoma 11, el cual proporciona las instrucciones para sintetizar una proteína esencial en el control de la división celular y la reparación de roturas de doble cadena de ADN.
Cuando este proceso de reparación celular falla, se genera una inestabilidad genómica que explica la tríada de neurodegeneración, inmunodeficiencia y el elevado riesgo de cáncer que presentan estos pacientes.
La manifestación clínica más temprana y característica es la ataxia cerebelosa progresiva, que suele detectarse entre los 1 y 4 años de edad, justo cuando el niño comienza a caminar; aunque inicialmente puede parecer torpeza motora, la inestabilidad empeora con el tiempo.
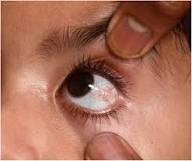
A nivel ocular, es común observar la apraxia oculomotora, descrita como la dificultad para iniciar movimientos oculares voluntarios que obliga al niño a girar la cabeza antes que los ojos. Posteriormente, entre los 4 y 6 años, aparecen las telangiectasias conjuntivales, que son vasos sanguíneos dilatados en los ojos que constituyen un rasgo definitivo de la enfermedad.
Neurológicamente, el cuadro clínico se completa con disartria, temblor de intención y movimientos coreoatetoideos, destacando que estos pacientes suelen presentar arreflexia o hiporreflexia debido a una neuropatía periférica, a diferencia de la hiperreflexia que se observa en otros trastornos cerebrales.
En el ámbito inmunológico, entre el 60% y el 80% de los pacientes desarrollan inmunodeficiencia humoral, manifestada principalmente por la deficiencia de IgA y niveles variables de deficiencia de IgG, lo que los hace altamente susceptibles a infecciones sinopulmonares recurrentes como la neumonía.
Para el diagnóstico, el hallazgo laboratorial más específico es la elevación marcada de la alfa-fetoproteína (AFP) sérica, presente en más del 95% de los casos con niveles de 10 a 100 veces por encima de lo normal. Aunque la resonancia magnética (RM) es fundamental para identificar la atrofia cerebelosa (especialmente del vermis), el estándar de oro para la confirmación diagnóstica es el análisis genético de las mutaciones del gen ATM.
Es una prioridad médica recordar que estos pacientes poseen una sensibilidad extrema a la radiación ionizante, por lo que se deben evitar las tomografías computarizadas (TC) y preferir siempre la RM.
El manejo de la ataxia-telangiectasia es fundamentalmente sintomático y multidisciplinario, ya que actualmente no existe una cura o tratamiento que modifique el curso de la enfermedad. El enfoque terapéutico incluye fisioterapia intensiva y el uso de equipos adaptativos para maximizar la independencia funcional, así como la terapia de reemplazo con inmunoglobulina (intravenosa o subcutánea) para aquellos con deficiencia de anticuerpos e infecciones frecuentes. Asimismo, la vigilancia oncológica es vital, dado que estos niños tienen un riesgo del 25% de por vida de desarrollar malignidades, siendo la leucemia y el linfoma las más prevalentes en la infancia.
La principal causa de mortalidad es la insuficiencia respiratoria, producto de una combinación de infecciones, riesgo de aspiración por disfagia y enfermedad pulmonar restrictiva por debilidad neuromuscular. La expectativa de vida suele situarse entre los 20 y 30 años, y dado el patrón de herencia, los hermanos de un afectado tienen un 25% de probabilidad de padecer la condición, lo que subraya la importancia del asesoramiento genético para la familia.
El panorama del tratamiento ha alcanzado un punto de inflexión histórico con los resultados del ensayo pivotal de fase III IB1001-303 promovido por IntraBio. Este estudio evaluó la levacetylleucine, una forma modificada del aminoácido leucina, demostrando una mejoría estadísticamente significativa en la escala SARA (Scale for the Assessment and Rating of Ataxia) de -1,88 puntos frente a placebo tras 12 semanas. Hallazgos adicionales presentados en el Congreso Internacional MDS 2025 sugieren que este fármaco podría frenar la progresión de la enfermedad, apuntando a un posible efecto neuroprotector. Actualmente, IntraBio ha presentado ante la FDA una solicitud de nuevo fármaco suplementaria (sNDA) para comercializar la levacetylleucine bajo el nombre de AQNEURSA®, lo que constituiría la primera aprobación regulatoria específica para la ataxia-telangiectasia.
Este avance contrasta con el reciente revés del ensayo NEAT, el estudio de fase III más grande realizado en A-T hasta la fecha, que evaluó el sistema EryDex. Esta tecnología consistía en la encapsulación de fosfato sódico de dexametasona en eritrocitos autólogos. A pesar de ser bien tolerado, el ensayo no alcanzó la significación estadística en sus objetivos primarios y secundarios, planteando interrogantes sobre si las estrategias antiinflamatorias por sí solas son suficientes o si se deben priorizar mecanismos terapéuticos alternativos.
Más allá de los ensayos en fase avanzada, el pipeline de investigación incluye líneas prometedoras como la terapia génica, que busca abordar la causa causal en el gen ATM, aunque todavía enfrenta retos en la transducción eficiente de neuronas cerebelosas. Otras moléculas en desarrollo son el MBM-01 (Tempol), un modulador del estrés oxidativo que busca reducir las roturas de ADN, y la pioglitazona (agonista PPAR-γ), que ha despertado interés por su capacidad para corregir déficits mitocondriales y restaurar niveles de glutatión. Asimismo, el triheptanoin se investiga para modular la disfunción mitocondrial pulmonar.
En conclusión, la ataxia-telangiectasia está dejando de ser una enfermedad huérfana en términos de tratamiento. Mientras que el manejo tradicional ha sido multidisciplinar para controlar las complicaciones oncológicas e inmunológicas, la posible aprobación de la levacetylleucine por agencias como la FDA y la EMA marca el inicio de una era de terapias con efecto sintomático-modificador.
