La Distrofia Muscular de Duchenne (DMD) representa uno de los desafíos más significativos en el ámbito de la neurología pediátrica. Se define como un trastorno neuromuscular de herencia recesiva ligada al cromosoma X, lo que explica por qué afecta predominantemente a varones, con una incidencia de aproximadamente uno de cada 3,500 nacimientos masculinos a nivel global. Esta condición no es simplemente una debilidad muscular progresiva. Es una carrera contra el tiempo que requiere una intervención clínica precisa desde los primeros años de vida para cambiar el curso natural de la enfermedad.
El origen de esta patología reside en una mutación en el gen DMD, el cual es responsable de codificar la distrofina. Esta proteína actúa como un amortiguador estructural esencial que conecta el citoesqueleto de la fibra muscular con la matriz extracelular. En los niños con Duchenne, la ausencia o deficiencia severa de distrofina provoca que la membrana muscular sea extremadamente frágil, derivando en una inestabilidad sarcolémica. Con cada contracción muscular, se producen microlesiones que el cuerpo no puede reparar adecuadamente, lo que lleva a una degeneración progresiva de las fibras y su posterior sustitución por tejido adiposo y conectivo.
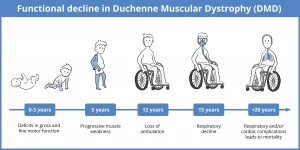
Identificar los primeros signos es crucial, ya que los síntomas suelen pasar desapercibidos durante la lactancia. El rango de edad crítico para el diagnóstico suele situarse entre los 2 y los 5 años. Es común que los padres noten que su hijo es más “torpe” que sus pares o que ha tardado más de lo habitual en caminar. Uno de los signos patognomónicos más reveladores es la Maniobra de Gower, donde el niño debe “caminar” con sus manos sobre sus propias piernas para poder incorporarse desde el suelo. Este fenómeno es una respuesta compensatoria directa a la debilidad de los músculos proximales, específicamente de los extensores de la cadera y la rodilla. Además, la pseudohipertrofia de las pantorrillas suele confundir a los familiares, quienes perciben unos gemelos fuertes cuando, en realidad, el músculo ha sido reemplazado por grasa.
Más allá de lo motriz, es fundamental entender que la DMD es una enfermedad sistémica. Entre el 50% y el 70% de los pacientes presentan retrasos en el habla y el lenguaje, debido a que la distrofina también cumple funciones en el desarrollo del sistema nervioso central. Esto subraya la necesidad de que cualquier retraso en el neurodesarrollo, incluso antes de que aparezca la debilidad muscular evidente, sea evaluado bajo la sospecha de una distrofia. En el laboratorio, el marcador de sospecha más potente es la Creatina Quinasa (CK), que en estos niños alcanza niveles estratosféricos, situándose entre 50 y 200 veces por encima de los valores normales, reflejando el daño muscular masivo y constante.
El diagnóstico definitivo ha evolucionado significativamente. Mientras que antes se dependía de la biopsia muscular, hoy en día las pruebas genéticas son la primera línea de acción, permitiendo identificar la mutación específica mediante técnicas de secuenciación de nueva generación. Este nivel de precisión es vital no solo para confirmar la enfermedad, sino para determinar si el paciente es candidato a terapias de vanguardia como la terapia de omisión de exón (Exon Skipping). Estos tratamientos innovadores, como el eteplirsen o el golodirsen, buscan restaurar el marco de lectura del gen para permitir la producción de una proteína más corta pero funcional, transformando potencialmente un fenotipo de Duchenne en uno más leve.
El manejo actual de la enfermedad se basa en un enfoque multidisciplinario proactivo. El estándar de oro sigue siendo la administración temprana de corticoesteroides (como prednisona o deflazacort), los cuales han demostrado ser eficaces para prolongar la deambulación independiente y retrasar las complicaciones respiratorias y cardíacas. No obstante, el cuidado debe ser integral: la vigilancia de la miocardiopatía dilatada mediante ecocardiogramas anuales y el inicio de pruebas de función pulmonar a partir de los 6 años son pasos indispensables para mejorar la supervivencia.
El manejo farmacológico de la Distrofia Muscular de Duchenne (DMD) ha evolucionado para convertir a los corticosteroides en la piedra angular del tratamiento, siendo el único fármaco que ha demostrado fehacientemente retrasar la progresión de la debilidad muscular. La comunidad médica internacional coincide en que el momento óptimo para iniciar esta terapia es durante la fase de meseta del desarrollo motor, que suele ocurrir entre los 4 y 6 años de edad, justo antes de que comience el declive funcional evidente.
En cuanto a la pauta específica, los dos fármacos más utilizados son la Prednisona (o Prednisolona) y el Deflazacort. Para la Prednisona, la dosis estándar recomendada es de 0,75 mg/kg al día, mientras que para el Deflazacort la dosis se ajusta a 0,9 mg/kg al día. Aunque históricamente se han ensayado pautas intermitentes —como 10 días de tratamiento seguidos de 10 días de descanso— para intentar reducir los efectos secundarios, los estudios clínicos más recientes, como el ensayo FOR-DMD, sugieren que la administración diaria continua es superior en cuanto a la preservación de la fuerza muscular y la función pulmonar a largo plazo. El Deflazacort suele preferirse en algunos centros debido a que se asocia con una menor ganancia de peso en comparación con la prednisona, aunque puede tener un impacto ligeramente mayor en el retraso del crecimiento lineal y la aparición de cataratas.
El tratamiento con esteroides no está exento de desafíos y exige una vigilancia estrecha de los efectos secundarios. Es imperativo que el equipo médico gestione de forma proactiva la salud ósea, ya que el uso crónico de corticoides aumenta el riesgo de osteoporosis y fracturas vertebrales. Por ello, se prescribe de forma rutinaria suplementación con Calcio y Vitamina D, junto con densitometrías óseas periódicas. Asimismo, el control nutricional es vital para evitar la obesidad, que podría sobrecargar aún más unos músculos ya debilitados, y se debe realizar un seguimiento oftalmológico para detectar la formación de cataratas subcapsulares posteriores.
Más allá de los fármacos, el abordaje integral requiere una fisioterapia especializada y constante. El objetivo principal de la terapia física no es el fortalecimiento intensivo, que podría ser contraproducente y dañar más las fibras musculares, sino el mantenimiento del rango de movimiento. Se hace especial énfasis en los estiramientos pasivos diarios para prevenir las contracturas en flexión, particularmente en el tendón de Aquiles y la fascia lata. El uso de férulas nocturnas es una práctica estándar para mantener los pies en una posición neutra y prolongar la capacidad del niño para caminar de forma independiente.
El soporte cardiopulmonar es otro pilar que define la esperanza de vida en la DMD. Dado que la afectación del músculo cardíaco es inevitable, las guías clínicas actuales recomiendan iniciar el tratamiento con inhibidores de la enzima convertidora de angiotensina (IECA) o bloqueadores de los receptores de angiotensina incluso antes de que aparezcan signos evidentes de disfunción en el ecocardiograma, a menudo a partir de los 10 años. En el plano respiratorio, cuando la capacidad vital forzada desciende por debajo de ciertos umbrales, se introduce el uso de máquinas de asistencia de la tos y ventilación no invasiva (BiPAP) nocturna, lo que previene infecciones respiratorias graves y mejora significativamente la calidad del sueño y la energía diaria del paciente.
Finalmente, el horizonte terapéutico se ha expandido con la llegada de la medicina de precisión. Además de los esteroides, hoy hablamos de la terapia de omisión de exón, diseñada para mutaciones específicas que permiten “saltarse” un error en el código genético y producir una forma funcional de distrofina. A esto se suma la reciente aprobación de terapias génicas mediante vectores virales, que buscan introducir un gen de “micro-distrofina” directamente en las células musculares. Estos avances, combinados con una nutrición adecuada, soporte psicológico y un manejo ortopédico cuidadoso, están transformando la DMD de una enfermedad puramente degenerativa a una condición crónica controlada con una expectativa de vida que ya alcanza la tercera y cuarta década.
