El Síndrome de Noonan se clasifica dentro del grupo de las rasopatías, un conjunto de trastornos del desarrollo causados por mutaciones en la vía de señalización RAS-MAPK. Esta vía es fundamental para la regulación de la proliferación y diferenciación celular, y su desregulación explica gran parte de las anomalías multisistémicas del síndrome. A nivel genético, la causa más común es una mutación en el gen PTPN11, presente en aproximadamente el 50% de los casos, aunque otros genes como SOS1, RAF-1 y RIT1 también juegan un papel crucial. Su herencia es autonómica dominante, pero presenta una expresividad variable, lo que significa que los síntomas pueden diferir significativamente incluso entre miembros de una misma familia.
Diagnóstico Clínico y Fenotipo Facial
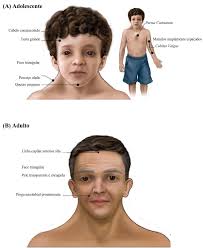
Para establecer un diagnóstico preciso, la medicina actual se apoya en el sistema de puntuación de Van der Burg, que evalúa criterios mayores y menores. Los rasgos faciales son distintivos, especialmente en la infancia, destacando las fisuras palpebrales inclinadas hacia abajo, orejas de implantación baja con rotación posterior e hipertelorismo (ojos muy separados). Es común observar también ptosis palpebral y un paladar ojival. Es vital que el clínico comprenda que estos rasgos faciales tienden a volverse más sutiles con la edad, lo que puede dificultar el diagnóstico en pacientes adultos si no se realizó en etapas tempranas.
Deformidades Torácicas y Sistema Linfático
Una de las manifestaciones físicas más características es la conformación del tórax. Los pacientes suelen presentar una combinación única de pectus carinatum en la parte superior y pectus excavatum en la inferior. Esto se acompaña del llamado tórax en escudo, donde los pezones se encuentran ampliamente separados, una condición presente en hasta el 95% de los pacientes. Además, a nivel circulatorio periférico, es frecuente el linfedema congénito en manos y pies durante la etapa de lactante, aunque este suele resolverse de forma espontánea durante la infancia temprana.
Compromiso Cardiovascular y Seguimiento
La afectación cardíaca es el factor que más influye en el pronóstico a largo plazo. La alteración de la vía RAS-MAPK interfiere directamente en la septación y formación de las válvulas durante el desarrollo embrionario. El defecto más frecuente es la estenosis pulmonar (50-60%), seguida de la miocardiopatía hipertrófica (20-30%). Debido a este riesgo, el protocolo estándar exige un ecocardiograma anual durante toda la infancia y adolescencia, espaciando las revisiones a cada 5 años en la edad adulta, complementado siempre con un electrocardiograma (ECG) anual.
Crecimiento, Desarrollo y Terapia Hormonal
Aunque la longitud al nacer suele ser normal, los pacientes desarrollan un retraso del crecimiento posnatal progresivo. Esto se traduce en una talla baja adulta promedio de 151 cm en mujeres y 162 cm en hombres. Para mitigar este efecto, la terapia con Hormona de Crecimiento (GH) está aprobada por la FDA para mejorar la estatura final, independientemente de si existe o no una deficiencia hormonal intrínseca. En el ámbito cognitivo, la mayoría de los pacientes sitúan su coeficiente intelectual entre 70 y 100, aunque es frecuente encontrar retrasos en el habla y dificultades específicas de aprendizaje que requieren apoyo pedagógico temprano.
Riesgos Hematológicos y Oncológicos
El manejo quirúrgico de estos pacientes exige precaución extrema debido a los trastornos de coagulación, presentes en la mayoría de los casos. La anomalía más recurrente es la deficiencia del Factor XI (55%), junto con la enfermedad de Von Willebrand y disfunciones plaquetarias. Por ello, es obligatorio realizar un cribado de coagulación exhaustivo antes de cualquier cirugía o procedimiento dental invasivo. Asimismo, existe un riesgo elevado de neoplasias hematológicas, particularmente la Leucemia Mielomonocítica Juvenil (LMMJ) y la Leucemia Linfoblástica Aguda (LLA), especialmente vinculadas a mutaciones en el gen PTPN11.
Manejo Clínico Específico y Pruebas Genéticas
En los varones, la criptorquidia (testículos no descendidos) afecta a más del 60%, siendo necesaria la orquidopexia entre los 6 y 18 meses para intentar preservar la fertilidad futura. Durante la lactancia, el 70% de los niños presentan dificultades de alimentación y disfagia, lo que requiere un manejo nutricional multidisciplinar hasta que los síntomas mejoran, generalmente hacia los 2 años. En cuanto a la confirmación diagnóstica, el abordaje preferido es un panel multigenético de rasopatías. Es importante recordar que una prueba genética negativa no excluye el diagnóstico si el paciente cumple con los criterios clínicos de Van der Burg, ya que aún existen mutaciones por identificar.
